为明确肺癌组织中不同细胞是否存在特异性微生物分布特征,本研究对两个公共数据集(LUAD-Set1和LUAD-Set2)进行分析,这两个数据集分别包含5例肺腺癌组织和5例配对正常肺组织的单细胞转录组测序数据。采用CellRanger和Seurat分析工具,在默认参数下将LUAD-Set1的细胞分为11个主要聚类(图1A,左)。通过SAHMI分析流程,从宿主组织的单细胞转录组测序数据中识别微生物信号。在鉴定出的533个微生物类群中,34个丰度最高类群在不同细胞类型中的分布特征见图1A(右)。研究发现,赖氨酸芽孢杆菌属、嗜麦芽窄食单胞菌属、魏斯氏菌属、丛毛单胞菌属和气单胞菌属这5个细菌属在肺腺癌和正常组织中的丰度存在显著差异。其中,赖氨酸芽孢杆菌属和嗜麦芽窄食单胞菌属在肺腺癌组织中丰度更高,而魏斯氏菌属、丛毛单胞菌属和气单胞菌属在正常组织中丰度更高(图1B)。为便于讨论,本研究暂将赖氨酸芽孢杆菌属和嗜麦芽窄食单胞菌属归为“有害细菌”,将魏斯氏菌属、丛毛单胞菌属和气单胞菌属归为“有益细菌”。对这类有益/有害细菌进行UMAP分析发现,“有害细菌”更倾向于富集在髓系细胞中(图1C,左),而“有益细菌”则更多分布于淋巴系细胞中(图1C,右)。为明确上述细菌属在不同免疫细胞中的相对丰度,本研究分析了其在各免疫细胞群中占所有相关细菌的比例。结果显示,在LUAD-Set1数据集中,巨噬细胞中赖氨酸芽孢杆菌属和嗜麦芽窄食单胞菌属的占比,显著高于CD4+ T细胞和自然杀伤细胞。魏斯氏菌属在CD8+ T细胞中的丰度显著高于调节性T细胞和巨噬细胞,其在自然杀伤细胞中的占比也显著高于调节性T细胞;丛毛单胞菌属在自然杀伤细胞中的丰度显著高于调节性T细胞和粒细胞;气单胞菌属在CD8+ T细胞中的丰度显著高于调节性T细胞和粒细胞(图1D)。在LUAD-Set2数据集中,赖氨酸芽孢杆菌属在不同免疫细胞群中的分布未观察到显著差异;嗜麦芽窄食单胞菌属在巨噬细胞中的丰度仍显著高于CD8+ T细胞;魏斯氏菌属在CD8+ T细胞中显著富集,丰度高于髓系细胞;丛毛单胞菌属在自然杀伤细胞中的丰度显著高于巨噬细胞和粒细胞;气单胞菌属在CD8+ T细胞中的丰度同样显著高于粒细胞(图1E)。众所周知,在肿瘤免疫微环境中,调节性T细胞、巨噬细胞和粒细胞均为免疫抑制性细胞,而CD8+ T细胞和自然杀伤细胞为免疫刺激性细胞。
为探究细菌在不同细胞类型中的异质性分布是否影响肿瘤免疫状态,本研究进一步分析了这5个细菌属的存在与宿主细胞基因表达是否存在关联。研究通过威尔科克森检验,结合细菌与宿主细胞的条形码配对,鉴定出与特定细菌相关细胞中的差异表达基因。在LUAD-Set1数据集中,与赖氨酸芽孢杆菌属、嗜麦芽窄食单胞菌属、魏斯氏菌属、丛毛单胞菌属、气单胞菌属相关的细胞,其差异表达基因数量分别为21、48、75、21和18个;在LUAD-Set2数据集中,上述对应数值则分别为323、53、55、86和36个。研究利用这些差异表达基因进行了基因本体富集分析。结果显示,整体而言,与赖氨酸芽孢杆菌属或嗜麦芽窄食单胞菌属相关的细胞,其富集的信号通路多与肿瘤进展相关,包括免疫抑制通路;而与魏斯氏菌属、丛毛单胞菌属或气单胞菌属相关的细胞,富集的则是与肿瘤抑制相关的通路,包括抗肿瘤免疫激活通路(图1F、G)。与赖氨酸芽孢杆菌属和嗜麦芽窄食单胞菌属相关的细胞,其富集通路主要为髓系细胞的活化与迁移、脂质的合成、转运和储存通路,这些通路被认为与肿瘤不良预后相关。与魏斯氏菌属、丛毛单胞菌属和气单胞菌属相关的细胞,其富集通路则多与抗肿瘤免疫激活或肿瘤细胞增殖抑制相关,如抗原提呈、细胞毒性T细胞活化、淋巴细胞分化及细胞周期调控等通路。据此,本研究初步推测,赖氨酸芽孢杆菌属和嗜麦芽窄食单胞菌属可能会促进肺腺癌的进展,而魏斯氏菌属、丛毛单胞菌属和气单胞菌属则可能发挥抑制肺腺癌的作用,这一结论与已有研究报道相一致。
为最终阐明这类细菌对肺腺癌进展的影响,以及在人类和小鼠中是否存在一致的作用规律,本研究采用瘤内直接注射细菌悬液的实验方法进行验证。实验选取了上述五个菌属中已报道存在于人体的菌株,即球形赖氨酸芽孢杆菌(L.sphaericus)、嗜麦芽窄食单胞菌(S.maltophilia)、食窦魏斯氏菌(W.cibaria)、睾丸丛毛单胞菌(C.testosteroni)和维氏气单胞菌(A.veronii),后续仍分别简称为赖氨酸芽孢杆菌属、嗜麦芽窄食单胞菌属、魏斯氏菌属、丛毛单胞菌属和气单胞菌属。具体操作为:当小鼠皮下LLC肿瘤体积长至约40mm³时,向瘤内注射100μL含5×10⁶个细菌的PBS缓冲液,随后监测肿瘤生长体积变化(图1H)。与PBS对照组相比,魏斯氏菌属组和丛毛单胞菌属组的肿瘤体积约减少1/3(P值分别为0.0273和0.0628),而赖氨酸芽孢杆菌属组和嗜麦芽窄食单胞菌属组的肿瘤体积则显著增大(图1I)。在细菌注射后的10天观察期内,小鼠体重整体呈上升趋势,无下降情况(图1J),表明该剂量的细菌注射未对小鼠造成损伤。魏斯氏菌属组的总T细胞比例显著高于PBS对照组,赖氨酸芽孢杆菌属组和嗜麦芽窄食单胞菌属组的总T细胞比例则相对较低(图1K),且该组的CD4+ T细胞总比例显著低于对照组、赖氨酸芽孢杆菌属组和气单胞菌属组,值得注意的是,气单胞菌属组的总T细胞比例呈下降趋势;CD8+ T细胞的总比例在各组间无显著差异,但魏斯氏菌属组和丛毛单胞菌属组中CD69+CD8+ T细胞(即活化的CD8+ T细胞)的比例显著高于对照组,而赖氨酸芽孢杆菌属组和嗜麦芽窄食单胞菌属组则呈现出截然相反的趋势(图1L);魏斯氏菌属组和丛毛单胞菌属组中调节性T细胞的比例显著低于其他各组(图1M)。与PBS对照组相比,魏斯氏菌属组中肿瘤相关巨噬细胞的总比例显著降低(图1N),魏斯氏菌属组和丛毛单胞菌属组中M1型巨噬细胞的比例显著升高,赖氨酸芽孢杆菌属组和嗜麦芽窄食单胞菌属组则显著降低(图1O),而M2型巨噬细胞的比例在各组间呈现出基本相反的变化趋势(图1P)。因此,赖氨酸芽孢杆菌属组和嗜麦芽窄食单胞菌属组的M1/M2型巨噬细胞比值较低,而魏斯氏菌属组和丛毛单胞菌属组的该比值较高(图1Q)。综上,在小鼠模型中,赖氨酸芽孢杆菌属和嗜麦芽窄食单胞菌属对肿瘤免疫微环境发挥抑制作用,进而促进肺腺癌进展,而魏斯氏菌属和丛毛单胞菌属则对肿瘤免疫微环境起到激活作用,从而抑制肺腺癌进展,这一结果与上述人类样本中的研究结果基本一致;但气单胞菌属在小鼠模型中并未表现出预期的免疫激活和肺腺癌抑制作用。

图1.解析肺腺癌中的肿瘤-免疫-微生物互作关系。(A)(左)LUAD-Set1数据集中肺腺癌组织(n=70,998个细胞)和正常组织(n=57,563个细胞)的宿主体细胞UMAP图;(右)肺腺癌和正常组织中丰度前34位的微生物类群(属水平)在细胞聚类中的分布(n=5)。(B)赖氨酸芽孢杆菌属、嗜麦芽窄食单胞菌属、魏斯氏菌属、丛毛单胞菌属和气单胞菌属在肺腺癌和正常组织中的独特计数(n=5),数据以中位数和95%置信区间(95%CI)表示,采用威尔科克森检验。(C)LUAD-Set1数据集中,赖氨酸芽孢杆菌属-嗜麦芽窄食单胞菌属-其他微生物(左)和魏斯氏菌属-丛毛单胞菌属-气单胞菌属-其他微生物(右)在肺腺癌和正常组织细胞聚类中的UMAP分布(n=5)。(D、E)分别为LUAD-Set1和LUAD-Set2数据集中,上述5个菌属的独特计数在9个免疫细胞聚类中的占比(n=5),采用方差分析和图基检验。(F、G)分别为LUAD-Set1和LUAD-Set2数据集中,含或不含上述5个菌属的细胞中差异表达基因(DEGs)的富集通路点图,点的大小按P值缩放。(H)体内细菌干预实验示意图。(I)各组LLC皮下肿瘤小鼠在观察期间的平均肿瘤体积(n=7)。(J)各组荷瘤小鼠在观察期间的平均体重(n=7)。(K-Q)流式细胞术分析各组肿瘤中T细胞(K)、CD69+CD8+ T细胞(L)、调节性T细胞(M)、肿瘤相关巨噬细胞(TAMs)(N)、M1型肿瘤相关巨噬细胞(O)、M2型肿瘤相关巨噬细胞(P)的比例及M1/M2比值(Q)(n=7),采用方差分析和图基检验。数据以平均值±标准误(Mean±SEM)和P值表示,ns表示无统计学差异。基于上述研究数据,本研究明确了两种促肿瘤细菌(赖氨酸芽孢杆菌属和嗜麦芽窄食单胞菌属)和两种抑肿瘤细菌(魏斯氏菌属和丛毛单胞菌属)。然而,将活菌直接注入体内作为治疗手段存在潜在安全风险。因此,本研究旨在筛选安全有效的化合物,该类化合物需能选择性清除促肿瘤细菌,同时促进抑肿瘤细菌生长,从而模拟有益细菌的功能作用。
为实现这一目标,本研究通过体外实验筛选了包含281种兼具抗菌和抗肿瘤活性的化合物库。当赖氨酸芽孢杆菌属、嗜麦芽窄食单胞菌属、魏斯氏菌属和丛毛单胞菌属达到对数生长期时,将其以1×105菌落形成单位(CFU)/孔的密度接种到96孔板中,并加入终浓度为0.1mmol/L的各化合物。以1%二甲基亚砜(DMSO)和50%二甲基亚砜分别作为阴性对照和阳性对照,孵育12-16小时后,通过检测600nm处的吸光度评估细菌存活率(图2A)。图2B展示了所有测试化合物对四种细菌存活率的影响,本研究将相对存活率低于25%定义为生长抑制阈值,相对存活率超过100%则视为具有细菌生长促进作用。
通过筛选确定了化合物集合的共同交集:97种抑制赖氨酸芽孢杆菌属的化合物、33种抑制嗜麦芽窄食单胞菌属的化合物、58种促进丛毛单胞菌属生长的化合物以及152种促进魏斯氏菌属生长的化合物(图2C)。最终获得两种交集化合物,即黄连素和万古霉素。检索这两种化合物的相关数据后发现,万古霉素引发耳毒性和肾毒性的概率较高,存在安全隐患,因此将其排除。后续研究聚焦于黄连素,重新验证其对四种细菌生长的影响,结果显示:黄连素对赖氨酸芽孢杆菌属和嗜麦芽窄食单胞菌属呈剂量依赖性抑制作用,半数抑制浓度(IC50)分别为0.02315mmol/L和0.02894mmol/L;而在不同浓度下,黄连素对魏斯氏菌属和丛毛单胞菌属的生长促进作用仍较为显著(图2D)。
在研究了黄连素的抗菌作用后,本研究进一步探究了其抗肺腺癌效果。CCK-8实验结果显示,黄连素能以剂量依赖方式有效抑制肺腺癌细胞增殖,其对LLC、H1975、H1299和A549细胞的IC50分别为66.69、28.63、38.74和46.00μmol/L(图2E),均低于其对赖氨酸芽孢杆菌属和嗜麦芽窄食单胞菌属的抑制浓度。以半数抑制浓度为参考,选用40μmol/L和80μmol/L的黄连素刺激H1299、A549、H1975和LLC细胞系,结果显示这些细胞集落形成能力显著减弱,且40μmol/L浓度下该减弱效应已十分明显(图2F)。随后,本研究检测了黄连素是否会诱导肺腺癌细胞凋亡,流式细胞术结果表明:H1299、H1975和LLC细胞经40μmol/L和80μmol/L黄连素处理48小时后,凋亡细胞比例显著升高;而人正常肺上皮细胞(HBE)的凋亡比例未超过10%,提示黄连素对正常肺上皮细胞仅具有轻微细胞毒性(图2G)。此外,本研究还探究了黄连素的体内抗肿瘤效果。已有研究表明,黄连素经腹腔注射的生物利用度显著高于口服/胃内给药。因此,对荷LLC皮下肿瘤的小鼠,每隔一天腹腔注射5mg/kg黄连素。观察终点(荷瘤第13天)时,治疗组小鼠的肿瘤体积较对照组减少40%以上(P=0.043)(图2H),且体重未出现下降(图2I)。综上,通过基于促肿瘤细菌和抑肿瘤细菌的高通量化合物筛选获得的微生物群调节剂——黄连素,在体内外均具有抗肺腺癌的潜力。

图2.通过药物筛选确定黄连素为优选微生物群调节剂。(A)药物筛选研究示意图。(B)0.1mmol/L化合物库刺激下,赖氨酸芽孢杆菌属、嗜麦芽窄食单胞菌属、丛毛单胞菌属和魏斯氏菌属相对存活率的散点图。(C)韦恩图展示抑制赖氨酸芽孢杆菌属、抑制嗜麦芽窄食单胞菌属、促进丛毛单胞菌属生长、促进魏斯氏菌属生长的四组化合物的重叠关系。(D)多种特定浓度黄连素刺激下,上述四种细菌的相对存活率(每个浓度n=8),标注半数抑制浓度(IC50)值。(E)多种浓度黄连素刺激下,赖氨酸芽孢杆菌属、嗜麦芽窄食单胞菌属、丛毛单胞菌属和魏斯氏菌属的相对存活率(每个浓度n=3),标注半数抑制浓度(IC50)值。(F)0、40和80μmol/L黄连素刺激下,H1299、A549、H1975和LLC细胞的克隆形成数(n=3),采用方差分析和图基检验。(G)0、40和80μmol/L黄连素处理48小时后,LLC、H1975、H1299和HBE细胞的凋亡比例(n=3),采用方差分析和图基检验。(H、I)磷酸盐缓冲液(PBS)组和黄连素组(5mg/kg,腹腔注射)荷LLC皮下肿瘤小鼠在观察期间的平均肿瘤体积(H)和平均体重(I)(n=10),采用Student’s t检验。数据以平均值±标准误(Mean±SEM)和P值表示,ns表示无统计学差异。
黄连素的水溶性较低(水中溶解度低于2.57mmol/L,二甲基亚砜中溶解度低于25mmol/L),这可能限制其在体内治疗相关浓度下的疗效。为解决这一局限性,本研究旨在寻找合适的生物载体以包裹黄连素。
在前期研究中,本团队通过自然孵育法已成功将甲氨蝶呤和氟伐他汀负载到肿瘤细胞来源微粒(TMPs)中,显著提高了这些药物的生物利用度。对荷LLC皮下肿瘤小鼠的体内成像数据显示,LLC细胞来源外泌体(LLC-EVs)的肿瘤组织靶向能力约为脂质体和间充质干细胞来源外泌体(MSC-EVs)的两倍(P<0.05)。基于这一发现,本研究选择LLC-EVs作为黄连素的生物载体。但由于黄连素溶解度低,自然孵育、超声处理等常规方法均无法将其有效负载到LLC-EVs中,因此采用电穿孔法作为替代负载策略(图3A)。重悬后,终产物呈现黄色胶体状,与空外泌体(EV-ctrl)存在明显差异,提示黄连素可能已成功载入。
随后,本研究采用多种技术对制备的制剂进行表征:EV-ber的zeta电位略低于EV-ctrl(图3B);纳米颗粒跟踪分析(NTA)显示,LLCEV-ctrl和H1975EV-ctrl的峰值粒径分别为149.5nm和161.2nm,而LLCEV-ber和H1975EV-ber的粒径略大,分别为186.3nm和177.9nm(图3C);电阻脉冲传感(RPS)法检测显示,相同样本的粒径分布范围更小(小于230nm),可能与RPS法对小粒径颗粒的检测灵敏度更高有关(图3D);透射电子显微镜(TEM)图像显示,EV-ctrl和EV-ber均呈不规则球形或杯状,粒径与NTA和RPS检测结果一致(图3E);蛋白质印迹(Westernblot)分析表明,EV-ber表达肿瘤细胞来源外泌体的四种经典标志物(CD9、CD63、EpCAM和肿瘤易感基因101蛋白(TSG101)),提示其经处理后仍保留了母细胞特性(图3F);EV-ber中未检测到钙连蛋白(Calnexin),表明其纯度良好(图3F);纳米流式细胞术(nFCM)分析也证实EV-ber表达CD9、CD63和EpCAM(图3G)。
采用高效液相色谱(HPLC)测定EV-ber中黄连素的精确含量,并通过包封效率(EE)和载药效率(LE)评估制备效果:包封效率定义为EV-ber中黄连素的重量(W)与初始黄连素重量(WBer)的比值,载药效率定义为EV-ber中黄连素的重量(W)与最终外泌体重量(WEV)的比值。基于标准曲线(图3I),当WEV:WBer比值分别为50:25、50:50、50:100、50:200和50:400时,黄连素的平均浓度分别为0.375、0.640、1.983、2.203和3.339μg/mL(图3H)。结果显示,随着体系中黄连素添加量的增加,载药效率(LE)逐渐升高,但包封效率(EE)显著下降(图3J),且外泌体损失率显著上升(图3K)。综合经济性考量,后续选择WEV:WBer=50:100的比值进行EV-ber制备,该条件下不仅载药效率适中,且包封效率最高、外泌体损失较少。
综上,本研究成功制备出负载特定量黄连素的EV-ber,且该制剂保留了外泌体的经典特征,同时确定了后续EV-ber制备的最佳WEV:WBer比值。
图3.负载黄连素的肿瘤细胞来源外泌体的制备与表征。(A)EV-ber制备示意图。(B)空外泌体(EV-ctrl)和EV-ber的zeta电位(n=3,采用Student’s t检验)。(C、D)分别通过NTA和RPS检测EV-ctrl和EV-ber的粒径分布。(E)TEM观察到的EV-ctrl(左)和EV-ber(右)的不规则球形或杯状形态。(F)Western-blot分析LLC细胞和EV-ber的外泌体阳性标志物与阴性标志物表达情况。(G)nFCM分析LLCEV-ber上CD9、CD63和EpCAM的表达。(H)HPLC检测不同WEV:WBer(μg)比值下,LLCEV-ber中黄连素的标准化浓度(n=3,采用方差分析和图基检验)。(I)HPLC检测不同浓度黄连素的峰面积标准曲线。(J)LLCEV-ber的包封效率和载药效率。(K)不同WEV:WBer(μg)比值下的外泌体损失率。数据以平均值±标准误(Mean±SEM)。
EV-ber的体外摄取效率、细胞毒性及体内生物分布评估
本研究随后评估了EV-ber的体外体内摄取效率及生物相容性。将1×105个LLC细胞分别用DAPI(标记细胞核)和PKH26(标记细胞膜)染色后,与60μg DiO标记的EV-ber共孵育。孵育1小时后,仅在LLC细胞周围观察到少量绿色颗粒状EV(图4A);而孵育24小时后,细胞膜被绿色荧光完全染色(图4B),表明所有LLC细胞均已与EV-ber融合。为精准测定摄取率,采用流式细胞术检测DiO标记EV-ber的绿色荧光阳性细胞比例,结果显示,孵育1、6、24小时的平均阳性率分别为1.81%、52.7%和95.9%(图4C)。这些体外实验结果表明,外泌体可有效与细胞膜融合并将药物递送至细胞内,且60μg外泌体与1×105个细胞共孵育24小时即可实现有效融合,提示后续细胞毒性分析应至少在孵育24小时后进行。
随后,本研究评估了EV-ber对LLC和H1975细胞的细胞毒性。实验设置PBS组、60μg/mL EV-ber组、60μg/mL空外泌体(EV-ctrl)组、常规剂量游离黄连素组(High Ber,100μmol/L~38.983μg/mL,约为半数抑制浓度的两倍)和EV-ber中等价黄连素剂量组(Ber,~1.2μg/mL),通过活/死细胞荧光染色和流式细胞术分析细胞凋亡情况。活/死细胞荧光染色结果显示,在LLC和H1975细胞中,High Ber组和EV-ber组的死细胞数量均显著高于PBS组、Ber组和EV-ctrl组(图4D-F);流式细胞术结果显示,High Ber组和EV-ber组的细胞凋亡率也显著升高,与活/死染色结果一致(图4G-I)。这些发现进一步证实EV-ber制备成功,且包裹的黄连素仍保留抗肿瘤活性,同时EV-ctrl组仅表现出微弱细胞毒性。得益于外泌体的高细胞摄取效率,仅需游离黄连素1/40的剂量,通过EV递送即可产生相当甚至更强的细胞毒性,凸显了外泌体作为药物递送载体的显著优势。
接下来,为探究EV-ber的体内生物分布,本研究向荷LLC皮下肿瘤小鼠分别通过灌胃(i.g.)、尾静脉注射(i.v.)和腹腔注射(i.p.)三种方式给予60μg DiR标记的EV-ber,随后进行体内成像。体内成像结果显示,给药后6小时,三组小鼠的荧光均主要定位于腹部区域,包括肝脏、消化道、脾脏和肾脏;给药后24小时,灌胃组荧光基本消散,而尾静脉注射组和腹腔注射组的荧光不仅仍存在于腹部脏器,还开始在胸腔区域(肺部)和肿瘤部位聚集(图4J)。
体外脏器成像进一步显示,给药后6小时,尾静脉注射组的肝脏和脾脏荧光强度最强,肺部也出现较强信号;而灌胃组和腹腔注射组的最强荧光则位于胃肠道,三组在其他脏器的荧光强度无明显差异(图4K、L)。给药后24小时,灌胃组仅在肝脏和肾脏检测到荧光;尾静脉注射组荧光仍集中于肝脏、脾脏和肺部;相比之下,腹腔注射组不仅在肝脏、脾脏、胃肠道和肺部均有荧光分布,且肿瘤部位的荧光聚集程度显著高于另外两组(图4K、M)。这些结果表明,腹腔注射的肿瘤靶向效果优于灌胃和尾静脉注射,其靶向性增强可能与EV-ber在肝脏和肺部的滞留时间较短、减少了单核吞噬细胞系统的清除有关。
此外,通过HPLC定量检测腹腔注射5mg/kg游离黄连素(High Ber组)和60μg EV-ber后肿瘤组织中的药物含量:High Ber组药物浓度随时间呈依赖性下降,而EV-ber组药物含量随时间逐渐升高;给药后9小时和12小时,EV-ber组的肿瘤组织药物浓度接近High Ber组的4倍(P<0.05;图4N),进一步证实EV-ber可有效将黄连素递送至肿瘤部位。综上,EV-ber在体内具有优异的肿瘤靶向能力,且腹腔注射是实现该靶向性的最优给药方式。
图4.EV-ber的体外摄取效率、细胞毒性及体内生物分布评估。(A、B)经红色膜染料PKH26预处理的LLC细胞,与绿色荧光染料DiO标记的EV-ber分别共孵育1小时(A)和24小时(B)的荧光成像。(C)流式细胞术检测DiO预染色EV-ber与1×105个LLC细胞共孵育1、6、24小时后的细胞内化效率(n=3)。(D)PBS,~1.2μg/mL黄连素(Ber),60μg/mL空外泌体(EV-ctrl),38.983μg/mL高剂量游离黄连素(High Ber)或60μg/mL EV-ber处理48小时后,LLC和H1975细胞的活/死荧光染色代表性图像(绿色为活细胞,红色为死细胞)。(E、F)分别为LLC(E)和H1975(F)细胞的死细胞比例(n=3,采用方差分析和图基检验)。(G)流式细胞术凋亡分析的代表性门控图。(H、I)上述五种处理方式作用48小时后,LLC(H)和H1975(I)细胞的凋亡率(n=3,采用方差分析和图基检验)。(J、K)DiR标记EV-ber经灌胃(i.g.)、尾静脉注射(i.v.)和腹腔注射(i.p.)给药后,6小时和24小时的体内荧光聚集图像(J)及体外脏器荧光成像(K)。(L、M)给药后6小时(L)和24小时(M)主要脏器的辐射效率结果(每个时间点n=3)。(N)高效液相色谱(HPLC)分析腹腔注射5mg/kg游离黄连素和60μg EV-ber后,不同时间点肿瘤组织中的黄连素浓度(每个时间点n=3,采用方差分析和图基检验)。
本研究随后评估了EV-ber的体内抗肺腺癌(LUAD)疗效。当LLC皮下肿瘤体积达到约30mm3时,将小鼠随机分为五个治疗组:游离黄连素的治疗剂量和给药途径与前期实验一致,即5mg/kg腹腔注射(High Ber组);空外泌体(EV-ctrl)组和EV-ber组均给予3mg/kg外泌体,基于HPLC分析,EV-ber中对应的黄连素含量为0.06mg/kg(Ber组)(图5A)。
PBS组、EV-ctrl组、Ber组、High Ber组和EV-ber组小鼠的中位生存期分别为23、23、21、27和27天(图5B)。整体对数秩检验显示五组小鼠的生存期存在显著差异(P<0.0001),Mantel-Cox检验表明PBS组与EV-ber组、High Ber组之间均存在统计学显著差异(P<0.0001)。另一项独立实验显示,经过五个治疗周期后,各组肿瘤大小出现显著差异(图5C):EV-ber组的平均肿瘤重量显著低于PBS组、EV-ctrl组和Ber组(图5D);且High Ber组和EV-ber组的肿瘤体积较PBS组、EV-ctrl组和Ber组均减少50%以上(图5E、F)。
为进一步阐明EV-ber介导的肿瘤抑制机制,本研究对五组小鼠的肿瘤组织进行了组织病理学分析,包括HE染色、增殖指数检测、微血管密度评估和TUNEL凋亡检测。对石蜡包埋切片分别进行Ki67抗体和CD31抗体免疫染色,以评估肿瘤细胞增殖能力和微血管密度;通过TUNEL assay检测凋亡细胞。HE染色结果显示,High Ber组和EV-ber组的肿瘤细胞核体积缩小、核染色变浅、胞质核比升高、伊红染色更均匀;此外,这两组的肿瘤细胞增殖能力和微血管密度均降低,而凋亡细胞数量增加(图5G)。
同时,本研究评估了EV-ber治疗的安全性。EV-ber组小鼠体重保持稳定,而High Ber组小鼠体重则呈现统计学显著的持续下降(图5H)。这一结果与前期实验(图2I)不一致,推测可能是由于黄连素水溶性低,High Ber溶液中添加的助溶剂在反复腹腔注射后引发慢性腹部炎症所致。两次实验中体重变化的差异表明,游离黄连素治疗的安全性仍不确定。但干预期末的检测显示,观察到的体重下降并未影响脏器功能:具体而言,五组小鼠的血清丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)、总胆红素(TBiL)和肌酐(Cr)水平无显著差异(图5I),表明所有治疗方案均未对肝肾功能造成不良影响;对小鼠心脏、肝脏、脾脏、肺和肾脏的死后组织病理学检查也显示,各治疗组均未出现形态学异常。
综上,在小鼠模型中,要达到与EV-ber相当的抗肺腺癌效果,游离黄连素的使用剂量需高达EV-ber的40倍。然而,如此高剂量游离黄连素的安全性仍存疑,这也凸显了EV-ber凭借其高效的肿瘤靶向能力所具备的安全性优势。
图5.EV-ber的体内安全性及抗肺腺癌效果评估。(A)皮下肿瘤模型构建后的治疗方案示意图。(B)接受PBS,0.06mg/kg黄连素(Ber),3mg/kg空外泌体(EV-ctrl),5mg/kg高剂量游离黄连素(High Ber)或3mg/kg EV-ber治疗的荷LLC皮下肿瘤C57小鼠的Kaplan-Meier生存曲线(n=8),采用Mantel-Cox检验。生存终点包括:自然死亡,肿瘤体积超过2000mm3,肿瘤最长直径超过20mm或体重下降超过20%。(C、D、E)经上述五种治疗12天后,荷LLC皮下肿瘤C57小鼠的肿瘤外观(C)、平均裸瘤重量(D)和平均肿瘤体积(E)(n=6),采用方差分析和图基检验。(F)五组荷瘤小鼠的肿瘤生长曲线。(G)肿瘤组织的HE染色,Ki67免疫组化染色,CD31免疫组化染色及TUNEL凋亡检测图像(TUNEL检测中绿色为凋亡细胞)。(H)经五种治疗12天后荷瘤小鼠的平均体重(n=6,采用方差分析和图基检验)。(I)经五种治疗12天后荷瘤小鼠的血清丙氨酸转氨酶(ALT),天冬氨酸转氨酶(AST),总胆红素(TBiL)和肌酐(Cr)水平(n=6)。生存观察和生长观察为两项独立实验。
EV‑ber重塑肿瘤免疫微环境并激活适应性免疫应答
已有研究表明,黄连素可激活CD8+ T细胞,并将M2型肿瘤相关巨噬细胞(TAMs)重新极化为具有炎症作用的M1型。因此,本研究进一步系统探究单独使用黄连素与EV‑ber在重塑肿瘤免疫微环境(TIME)中的作用,包括适应性免疫与固有免疫。
T细胞,尤其是CD8⁺ T细胞,是抗肿瘤免疫的核心效应细胞。因此,本研究首先检测了经PBS、Ber、EV‑ctrl、High Ber或EV‑ber处理12天后,小鼠LLC皮下肿瘤组织中总T细胞、CD4+ T细胞和CD8⁺ T细胞的分布与含量(图6A)。结果发现,与对照组相比,High Ber组和EV‑ber组的CD4+细胞与CD8⁺细胞均显著升高(图6B)。随后,本研究采用多色流式细胞术,更全面、准确地评估黄连素与EV‑ber对免疫微环境的影响。
结果显示,High Ber组和EV‑ber组均可显著提高树突状细胞(DCs)及成熟树突状细胞(mDCs)的浸润比例,而DC是启动抗肿瘤免疫的关键起始细胞(图6C、D)。更重要的是,尽管总T细胞与CD4+ T细胞的总体比例未见明显改变,但High Ber与EV‑ber处理均显著提升了活化T细胞(IFN‑γ⁺ T细胞)的比例(图6E),同时也显著提高了CD8⁺ T细胞及IFN‑γ⁺CD8⁺ T细胞的比例(图6F、G)。此外,被认为有利于抗肿瘤免疫的Th1细胞比例在处理后显著升高(图6H),而被认为不利于抗肿瘤免疫的Th2细胞与调节性T细胞(Treg)比例则显著降低(图6I、J)。作为固有淋巴细胞亚群之一,NK细胞目前被定义为与细胞毒性T细胞(CTL)功能类似的效应细胞,可通过抑制肿瘤细胞增殖、迁移及远处组织定植,对原发肿瘤和转移灶发挥天然细胞毒作用。结果显示,NK细胞与NKT细胞的总体比例无明显变化(图6K),但处理后NK细胞中CD69的平均荧光强度显著升高,提示活化NK细胞比例增加(图6L)。髓系细胞的变化主要体现为:M1型肿瘤相关巨噬细胞(M1‑TAMs)比例显著升高(图6M),M2型肿瘤相关巨噬细胞(M2‑TAMs)比例显著降低(图6N),M1/M2比值显著上升(图6O);而总肿瘤相关巨噬细胞(TAMs)、粒系髓源抑制细胞(G‑MDSCs)及单核系髓源抑制细胞(M‑MDSCs)的比例无显著变化。
已知促肿瘤性炎症会干扰正常髓系造血过程,从而产生MDSCs等免疫抑制性髓系细胞,进而抑制效应淋巴细胞功能。TAMs同样属于免疫抑制性髓系细胞,在肿瘤免疫微环境中发挥复杂作用:例如,M2型TAMs可通过促进血管生成、抑制T细胞功能来支持肿瘤生长,而M1型TAMs则可通过精氨酸代谢杀伤肿瘤细胞,发挥抗肿瘤作用。因此,处理后髓系细胞发生的一系列变化,共同表明肿瘤组织中正向抗肿瘤免疫微环境的形成。综上,本研究结果表明,单独使用黄连素和EV‑ber均能优化肿瘤免疫微环境,有利于抑制肺腺癌进展,这也解释了单独黄连素和EV‑ber在荷瘤小鼠中展现出的良好抑瘤效果。
图6.EV‑ber重塑肿瘤免疫微环境并激活适应性免疫应答。对荷LLC皮下肿瘤小鼠分别给予PBS,0.06mg/kg Ber,3mg/kg EV‑ctrl,5mg/kg High Ber或3mg/kg EV‑ber处理12天,取肿瘤组织,通过免疫组化或流式细胞术检测肿瘤免疫微环境中的免疫细胞。(A)肿瘤组织中CD3⁺、CD4⁺和CD8⁺细胞的代表性荧光图像。(B)肿瘤组织每视野CD4⁺和CD8⁺细胞计数(3只小鼠,共9个视野,采用方差分析和图基检验)。(C–O)多色流式细胞术检测肿瘤中各类细胞比例或比值:树突状细胞(DCs)(C),DCs的CD86平均荧光强度(MFI)(D),IFNγ⁺ T细胞(E),CD8⁺ T细胞(F),IFNγ⁺CD8⁺ T细胞(G),Th1细胞(H),Th2细胞(I),调节性T细胞(Tregs)(J),NK细胞(K),NK细胞的CD69平均荧光强度(L),M1型肿瘤相关巨噬细胞(M1‑TAMs)(M),M2型肿瘤相关巨噬细胞(M2‑TAMs)(N)及M1/M2比值(O)(n=5,采用方差分析和图基检验)。MFI:平均荧光强度。
在本研究初期我们已证实,人肺腺癌组织中存在一定数量的微生物,且在肿瘤内不同细胞群中呈不均匀分布,这类微生物被定义为肿瘤内微生物组;同时我们也证实,黄连素对不同细菌具有异质性作用,游离黄连素和负载黄连素的EV‑ber可在体内外发挥抗肺腺癌作用并重塑肿瘤免疫微环境。
因此,本部分旨在探究黄连素和EV‑ber是否能够影响小鼠肺腺癌的肿瘤内微生物组,及其与肿瘤免疫微环境的潜在关联。首先,通过绝对定量qPCR检测不同处理方案下荷瘤小鼠肿瘤组织中的细菌总载量。结果显示,与PBS组和EV‑ctrl组相比,High Ber组和EV‑ber组的平均细菌数量减少了近50万(图7A)。随后,对肿瘤组织进行脂多糖(LPS,革兰氏阴性菌特征成分)和脂磷壁酸(LTA,革兰氏阳性菌特征成分)免疫组化染色,以直观显示肿瘤内微生物组的变化(图7B)。利用Image J软件定量分析表明,与对照组相比,High Ber组和EV‑ber组的平均阳性面积(图7C)及平均光密度值均显著降低。将各组阳性面积数据以PBS组为基准归一化后,LPS与LTA的抑制程度无统计学差异(各组均P=0.7176)(图7D)。综上,结果表明游离黄连素和EV‑ber均可非选择性降低肿瘤内细菌总量,对革兰氏阳性菌与革兰氏阴性菌无明显偏向性。肿瘤内微生物总量下降(即细菌死亡)可能会激活抗肿瘤免疫,这在一定程度上解释了EV‑ber能够改善肿瘤免疫微环境的原因。
为进一步探究肿瘤内微生物组的具体变化,本研究进行了微生物组测序。由于肿瘤部位细菌含量极低,16S rDNA测序文库构建失败,但采用灵敏度与准确度更高的2bRAD‑M测序技术成功构建了文库。在α多样性方面,High Ber组和EV‑ber组的微生物群落丰度高于对照组(Chao指数,Wilcoxon检验,P=0.0959)(图7E,左)。基于Bray‑Curtis距离的非度量多维尺度分析(NMDS)进行β多样性分析,结果显示四组间的微生物组成存在明显差异(stress=0.173)(图7E,右)。LEfSe分析共筛选出14个组间相对丰度差异显著的特征物种(LDA评分≥2.0)(图7F)。
在研究较为充分的门水平上,本研究发现:EV‑ber处理后,梭杆菌门、软壁菌门、担子菌门等多种促肿瘤发生的类群丰度降低,而拟杆菌门等具有抗癌保护作用的益生菌类群丰度升高(图7G)。综上,包括EV‑ctrl在内的不同处理均会改变肿瘤内微生物组的组成;EV‑ber处理可增加“有益”微生物、减少“有害”微生物。为阐明黄连素和EV‑ber的治疗机制,本研究随后构建了清除肿瘤内细菌的皮下肿瘤模型(ABTx)。值得注意的是,清除肿瘤内细菌本身并未改变肿瘤进展(P=0.9015),但可显著削弱High Ber和EV‑ber的治疗效果(P值分别为0.0844和0.0511)。重要的是,在ABTx模型小鼠中,High Ber和EV‑ber仍表现出显著高于未治疗ABTx组的治疗效果(均P<0.0001;图7H)。ABTx模型对小鼠体重无影响,黄连素处理组出现的体重下降趋势与前期结果一致(图7I)。上述结果表明,黄连素和EV‑ber的治疗机制同时涉及肿瘤内微生物组调控与直接抗肿瘤作用。
随后,本研究探究了EV‑ber诱导的肿瘤内微生物组改变是否会影响肿瘤免疫微环境,以阐明黄连素和EV‑ber重塑肿瘤免疫微环境的机制。为明确与黄连素作用相关、且同时关联肿瘤内微生物与抗肿瘤免疫的特异性微生物和免疫靶点,我们对2bRAD‑M测序(简化宏基因组测序技术)数据进行了系统分析。在单因素方差分析(one‑way ANOVA)的多组间差异检验中,发现唾液普雷沃氏菌(Prevotella salivae)和变形链球菌(Streptococcus mutans)在High Ber组和EV‑ber组中的丰度显著高于PBS组和EV‑ctrl组(图7J)。Kruskal‑Wallis检验进一步证实,二氧化碳噬纤维菌口腔分类群329菌株F0087、卟啉单胞菌KLE_1280、唾液普雷沃氏菌在High Ber组和EV‑ber组中较对照组显著升高。
这些细菌类群在EV‑ber组与High Ber组中呈现一致的变化,提示该效应主要源于黄连素本身,而非其他混杂因素。在三种差异丰度的类群中,变形链球菌丰度最高(超过0.5%),提示其具有潜在生物学意义。近期研究表明,将变形链球菌引入治疗性生物材料可促进肿瘤免疫微环境中树突状细胞成熟与T细胞活化。我们推测,肿瘤内变形链球菌的增加可调控免疫细胞浸润。为排除混杂因素影响,将5×10⁶个变形链球菌直接注射至LLC皮下肿瘤内。结果令人意外:观察10天后,注射变形链球菌的小鼠肿瘤体积显著小于对照组(P=0.0449;图7K),且对体重无明显影响(图7L)。
随后收集肿瘤组织进行多色流式分析。与前期实验(图6)不同,本次观察到的免疫改变主要与适应性免疫相关:树突状细胞与成熟树突状细胞水平升高(图7M);总T细胞和CD8⁺ T细胞显著增加,同时CD4⁺ T细胞减少、CD4/CD8比值降低(图7N)。而在固有免疫细胞群中,包括肿瘤相关巨噬细胞(TAMs)、M1型TAMs、M2型TAMs及NK细胞,均未出现显著变化。此外,我们利用原代免疫细胞对上述结果进行了验证。
在变形链球菌存在的情况下,High Ber和EV‑ber均可显著提高骨髓来源树突状细胞(BMDCs)中CD86的表达水平(图7O)。在原代T细胞培养体系中,变形链球菌还可使CD4⁺ T细胞减少,CD69⁺CD8⁺ T细胞增加,但对总CD8⁺ T细胞无显著影响(图7P)。同时,变形链球菌可显著增强黄连素和EV‑ber促进骨髓来源巨噬细胞(BMDMs)向M1型极化、并抑制其向M2型极化的能力(图7Q)。值得注意的是,单独使用变形链球菌并未产生显著作用,这与体内实验结果一致。综上,本研究结果表明:EV‑ber可降低肿瘤内细菌总量、改变菌群组成,并通过调控肿瘤内微生物组影响特异性抗肿瘤免疫。这证实肿瘤内微生物组是EV‑ber作用于肿瘤免疫微环境的中间环节,与我们前期的假设一致。
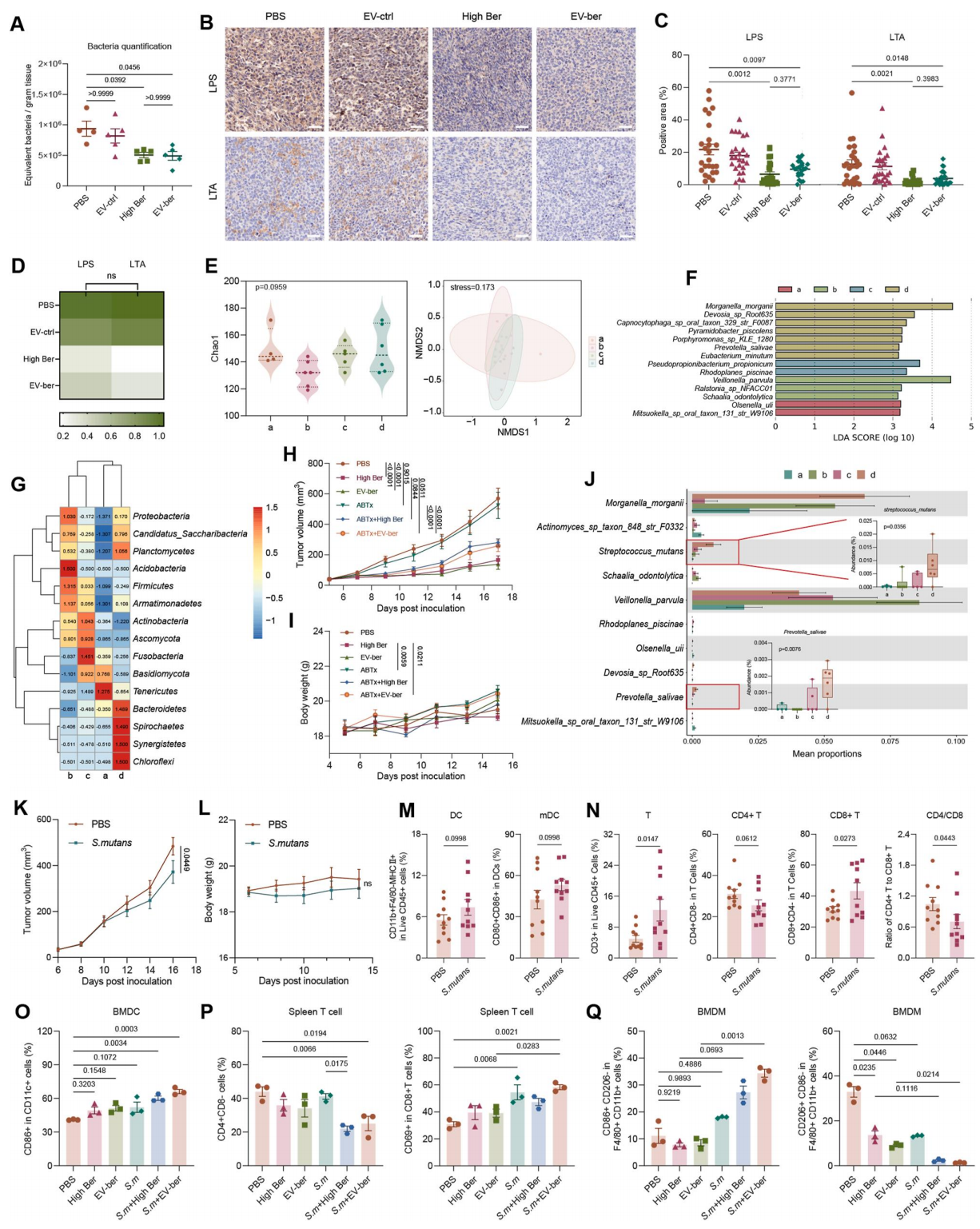
图7.EV‑ber调控肺腺癌肿瘤内微生物‑免疫网络。(A)针对V9区的绝对定量qPCR检测PBS,3mg/kg EV‑ctrl,5mg/kg High Ber,3mg/kg EV‑ber处理12天后,LLC皮下肿瘤组织中的细菌总量(n=4或5),采用Kruskal‑Wallis检验。IHC染色LPS和LTA以显示各组小鼠肿瘤内革兰氏阴性菌与革兰氏阳性菌含量。(B)各组LPS、LTA免疫组化染色代表性图像。比例尺:40μm。(C)LPS与LTA的阳性面积统计。(D)热图展示LPS与LTA的标准化阳性面积(5个样本,共25个视野),采用方差分析和图基检验。(E)四组微生物α多样性(Chao指数,Wilcoxon检验,左图)与β多样性(NMDS分析,右图)。(F)LEfSe分析揭示四组间在物种水平上相对丰度差异显著的特征物种。(G)热图展示四组在门水平上排名前30类群的相对丰度,标注G‑score值。(H、I)LLC皮下肿瘤小鼠经PBS,5mg/kgHigh Ber,3mg/kgEV‑ber,ABTx,ABTx+High Ber,ABTx+EV‑ber处理12天后的肿瘤体积(H)和体重(I)(n=6),采用方差分析和图基检验。(J)柱状图展示四组间类群相对丰度的差异,其中High Ber和EV‑ber组变形链球菌与唾液普雷沃氏菌显著升高(方差分析)。分组:a=PBS,b=EV‑ctrl,c=High Ber,d=EV‑ber,n=4–6。(K、L)PBS与5×10⁶个变形链球菌处理后,荷瘤小鼠的肿瘤体积(K)和体重(L),采用方差分析和图基检验。(M、N)流式细胞术检测PBS与变形链球菌组小鼠肿瘤浸润免疫细胞比例:(M)DCs与mDCs;(N)总T细胞、CD4⁺ T细胞、CD8⁺ T细胞及CD4/CD8比值(n=10),采用Student’s t检验。(O–Q)分别用PBS,38.983μg/mL黄连素(High Ber),60μg/mLEV‑ber,变形链球菌(MOI20:1),变形链球菌+High Ber,变形链球菌+EV‑ber处理18h后:(O)骨髓来源树突状细胞(BMDCs),(P)脾脏T细胞,(Q)骨髓来源巨噬细胞(BMDMs)的分化变化(n=3),采用方差分析和图基检验。
EV‑ber抑制肿瘤转移并增强抗PD‑L1抗体的抗肺腺癌活性
上述结果表明,小鼠皮下肿瘤中存在一定数量的细菌,且可被EV‑ber显著减少。近期研究显示,肿瘤驻留的胞内微生物(尤其是活菌)可促进乳腺癌的转移定植。基于此,本研究设计了改良实验方案,以评估EV‑ber通过降低肿瘤内微生物组发挥的抗转移作用(图8A)。简而言之:先在小鼠体内构建LLC‑GFP皮下肿瘤,培养20天使其形成稳定的肿瘤内微生物组;随后将肿瘤解离,通过荧光激活细胞分选(FACS)纯化去除其他细胞类型,只保留LLC‑GFP细胞;最后将这些纯化细胞尾静脉注射到另一批小鼠体内,建立转移模型。Fu等人的研究结果显示,近80%的肿瘤驻留微生物定位于细胞质中,这支持我们使用肿瘤细胞构建转移模型。经过近三周的转移形成期,我们观察到:注射经High Ber或EV‑ber处理的LLC‑GFP细胞的小鼠,全身转移灶数量显著更少(图8B),且总生存期显著延长(图8C)。由于肺是全身转移的主要部位,我们对每只小鼠的完整肺组织进行解剖并制作全肺石蜡切片。全肺HE染色结果与全身观察一致:与对照组相比,来自High Ber或EV‑ber处理组LLC‑GFP细胞的小鼠,肺转移负荷降低30%以上(图8D)。综上,这些结果证实:游离黄连素和EV‑ber均能有效抑制肿瘤转移。肿瘤微环境是一个复杂的系统,其中恶性细胞与免疫细胞和非免疫细胞单独或共同作用,影响免疫治疗的敏感性。鉴于High Ber和EV-ber可诱导肿瘤免疫微环境重塑,表现为成熟树突状细胞和CD8+ T细胞富集,我们通过评估肿瘤生长情况,探究游离黄连素和EV-ber是否能够增强抗PD-L1(αPD-L1)治疗的疗效。LLC荷瘤小鼠的治疗方案如图8E所示。值得注意的是,所有治疗组均未观察到体重明显下降(图8F)。肿瘤生长曲线和剥离肿瘤的代表性图像如图8G-I所示。平均肿瘤重量数据显示,单独使用αPD-L1可使肿瘤生长抑制近50%。重要的是,与单独使用αPD-L1、High Ber或EV-ber相比,αPD-L1分别联合High Ber或EV-ber可进一步增强治疗效果(图8J)。综上,这些发现突出了EV-ber作为提高αPD-L1治疗效果的联合策略具有潜力且安全性良好,体现了其广泛的治疗价值。

图8.EV‑ber抑制肿瘤转移并增强抗PD‑L1抗体的抗肺腺癌活性。(A)转移实验流程示意图。(B)小动物活体成像系统(IVIS)拍摄的小鼠全身转移灶图像,带勾的空白框表示在成像前已死亡的小鼠,图中展示了IVIS图像的辐射效率(n=7-11,采用方差分析和图基检验)。(C)转移形成约3周后转移模型小鼠的Kaplan‑Meier生存曲线(n=12,采用Mantel‑Cox检验)。(D)全肺石蜡包埋切片HE染色代表性图像及相应肺组织照片,以及肺转移面积统计结果(n=11,采用方差分析和图基检验)。(E)联合治疗实验流程示意图,High Ber与αPD‑L1的单次给药剂量均为5mg/kg。(F)接受PBS,High Ber,EV‑ber,αPD‑L1,αPD‑L1联合High Ber,αPD‑L1联合EV‑ber处理12天后荷瘤小鼠的平均体重(n=6,采用方差分析和图基检验)。(G)平均肿瘤体积。(H)荷瘤小鼠肿瘤生长曲线。(I)肿瘤大体形态。(J)裸瘤平均重量,采用方差分析和图基检验。数据以平均值±标准误(Mean±SEM)和P值表示,ns表示无统计学差异。